科济药业发布2023年度业绩
2024年3月26日,科济药业作为一家始终专注于治疗血液恶性肿瘤和实体瘤的创新CAR-T细胞疗法公司,发布了2023年度业绩。
科济药业创始人、首席执行官李宗海博士表示:“2023年,科济药业仍怀着‘科创济世’的愿景,致力于强化团队协作及提高经营效率。我们在创新产品注册及临床研究以及新技术平台推进方面取得重要进展。同时,我们在不同候选产品临床研究、注册及业务发展等方面达成多个重要里程碑。我们乐观地认为,我们将以韧性和决心面对及克服前方的挑战,推进我们的创新细胞疗法。”
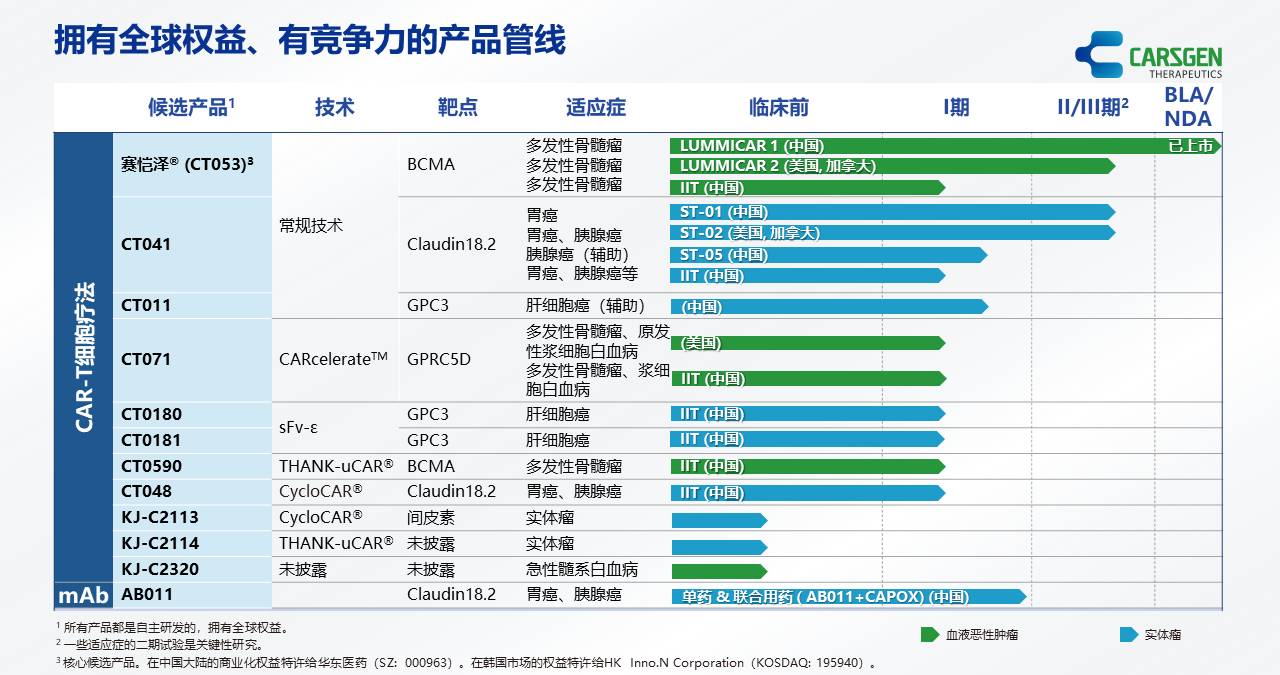
而赛恺泽(泽沃基奥仑赛注射液,CT053)是一种用于治疗复发或难治性多发性骨髓瘤的全人源B细胞成熟抗原(BCMA)自体CAR-T细胞候选产品。科济药业于2024 年3 月1日收到国家药品监督管理局的通知,附条件批准赛恺泽新药上市申请(批准日期2024年2月23日),用于治疗复发或难治性多发性骨髓瘤成人患者,既往经过至少3线治疗后进展(至少使用过一种蛋白酶体抑制剂及免疫调节剂)。在中国进行的I期试验(NCT03975907)的三年随访的更新数据于2023年12月在2023年美国血液学会(“ASH”)年会上以壁报形式展示。
CT041是一种靶向Claudin18.2(CLDN18.2)(一种在部分癌症中高表达的膜蛋白)的自体人源化CAR-T细胞候选产品。截至公告日期,根据我们的资料,CT041是世界上第一款进入II期临床试验的治疗实体瘤的CAR-T细胞候选药物。CT041已于2023年4月获得国家药品监督管理局的IND批准用于Claudin18.2表达阳性的胰腺癌术后辅助治疗(CT041-ST-05, NCT05911217)。2023年5月,美国和加拿大1b/2期临床试验(NCT04404595)的2期部分启动,用于治疗既往接受过至少二线治疗失败Claudin18.2表达阳性的晚期胃癌/食管胃结合部腺癌的患者。CT041在美国的1b期研究(NCT04404595)的更新数据在2024年美国临床肿瘤学会胃肠道肿瘤研讨会(“ASCO GI”)上以壁报形式展示。
CT011是一种靶向Glypican-3(GPC3)的自体CAR-T细胞候选产品。CT011已于2024年1月获得国家药品监督管理局的IND批准用于治疗手术切除后出现复发风险的GPC3阳性的IIIa期肝细胞癌患者。
CT071是一种靶向G蛋白偶联受体C组5成员D(GPRC5D)的自体全人源CAR-T细胞治疗候选药物,利用科济药业专有的CARcelerateTM平台开发,用于治疗复发或难治性多发性骨髓瘤(R/R MM)及复发/难治原发性浆细胞白血病(R/R pPCL)。CT071已于2023年11月30日获得FDA的IND批准用于治疗R/R MM及R/R pPCL。一项研究者发起的临床试验正在中国开展,旨在评估CT071治疗R/R MM及复发/难治浆细胞白血病(R/R PCL)(NCT05838131)的安全性和疗效。
2023年1月,科济药业和华东医药股份有限公司(股票代码:SZ.000963)全资子公司华东医药(杭州)有限公司关于在中国大陆地区商业化赛恺泽签订合作协议。
2023年8月,科济药业与美德纳公司(纳斯达克股票代码:MRNA,“美德纳”)已启动一项合作协议,以研究CT041与美德纳的试验性Claudin18.2 mRNA癌症疫苗的组合效果。
由此,科济药业建立了从靶点发现、创新型CAR-T细胞研制、临床试验到商业规模生产的CAR-T细胞研究与开发平台。我们通过自主研发新技术以及拥有全球权益的产品管线,以解决CAR-T细胞疗法的重大挑战,比如提高安全性,提高治疗实体瘤的疗效和降低治疗成本。科济药业的使命是成为能为全球癌症患者带来创新和差异化的细胞疗法,并使癌症可治愈的全球生物制药领导者。



